乳腺癌的發(fā)病率逐年增高,并成為中國女性發(fā)病率最高的惡性腫瘤,是人們常說的“紅顏殺手”。其中,三陰性乳腺癌惡性程度較高毙籽,患者生存預后較差,易出現(xiàn)早期復發(fā)和轉(zhuǎn)移,且既往缺乏有效的針對性治療策略悴晰,素有最“毒”乳腺癌之稱。近日逐工,復旦大學腫瘤醫(yī)院邵志敏教授铡溪、江一舟教授課題組攜手復旦大學基礎醫(yī)學院教育部/衛(wèi)健委/醫(yī)科院醫(yī)學分子病毒學重點實驗室趙超課題組,發(fā)現(xiàn)微生物代謝產(chǎn)物氧化三甲胺(TMAO)可以激活抗腫瘤免疫泪喊,提高三陰性乳腺癌免疫治療療效棕硫。這意味著微生物代謝產(chǎn)物TMAO有望成為三陰性乳腺癌臨床免疫治療的新策略,助推免疫治療窘俺。該項重要研究成果已在北京時間3月12日凌晨在國際權威期刊Cell Metabolism(《細胞代謝》)以封面文章發(fā)表饲帅。

研究借助多維組學分析發(fā)現(xiàn),三陰性乳腺癌患者中免疫調(diào)節(jié)亞型(Immunomodulatory, IM瘤泪。即灶泵,對免疫治療可產(chǎn)生應答組)的乳腺微環(huán)境中,梭菌目下菌屬的占比顯著高于其他亞型患者,提示瘤內(nèi)共生菌群可能與抗腫瘤免疫應答有關赦邻。結(jié)合代謝數(shù)據(jù)分析發(fā)現(xiàn)髓棋,梭菌相關代謝產(chǎn)物TMAO在IM亞型患者中的豐度更高,且與微環(huán)境內(nèi)CD8+ T細胞比例和gamma干擾素表達量成正相關轻樟。體內(nèi)外實驗證明趴国,組織內(nèi)TMAO誘導乳腺癌細胞發(fā)生由GSDME介導的焦亡,向微環(huán)境內(nèi)釋放大量炎性因子舟门,從而實現(xiàn)對腫瘤特異性CD8+ T細胞募集和功能活化债苍。同時發(fā)現(xiàn),TMAO可活化內(nèi)質(zhì)網(wǎng)應激相關的PERK蛋白锅星,繼而切割GSMDE的上游蛋白caspase-3誘導腫瘤細胞發(fā)生焦亡咳铅。通過給小鼠喂食TMAO前體物膽堿可提高血漿和瘤內(nèi)TMAO水平,激活三陰性乳腺癌抗腫瘤免疫家统,提高免疫治療療效具椒。因此,補充膽堿攝入可以作為提高三陰性乳腺癌免疫治療療效的臨床潛在治療策略曹均。
?
與常見文章報道的抗腫瘤激活劑直接作用于免疫細胞發(fā)揮作用不同斧壮,該研究從獨特角度出發(fā),發(fā)現(xiàn)特殊微生物群落借助代謝產(chǎn)物直接作用于腫瘤細胞纤悉,誘導其焦亡蔬咬,繼而促進免疫細胞浸潤,最終發(fā)揮抗腫瘤作用央渣。該研究计盒,提出一種菌群促進細胞微環(huán)境炎性浸潤的新機制,為提升特異性免疫應答效率提供了全新的思路芽丹。
?
“乳腺癌像一個‘大家族’北启,可細分為腔面A、腔面B拔第、HER-2陽性和三陰性四大亞型咕村,其中三陰性乳腺癌是最‘毒’的一種,”項目主要研究者邵志敏教授表示蚊俺,“三陰性乳腺癌占乳腺癌總體人群的10%-20%懈涛,其雌激素受體、孕激素受體以及HER-2表達均為陰性泳猬。與其他三種乳腺癌亞型相比批钠,三陰性乳腺癌患者生存預后較差〉梅猓”
近年來了岸,以PD-1抑制劑為代表的免疫治療成為三陰性乳腺癌頗具前景的治療手段颗屏。但即便如此,隨著臨床研究的不斷深入造蒋,仍有相當一部分患者難以從免疫治療中獲益卑托。為了進一步提高精準治療療效,復旦大學腫瘤醫(yī)院邵志敏教授篱辫、江一舟教授團隊于2019年提出“復旦分型”势粱,發(fā)現(xiàn)三陰性乳腺癌中有一類獨特的免疫調(diào)節(jié)亞型(Immunomodulatory, IM),其患者有較為活化的免疫微環(huán)境特征彪珍,能夠從免疫治療中獲益食土。“如何提高三陰性乳腺癌免疫治療療效讽钻,是亟待解決的臨床難題赵须。”邵教授評價道扎矾。
獨特視角揭示新策略:小小細菌成免疫治療關鍵“援軍”
既往研究中,各國科學家從人體本身的角度對免疫治療進行研究倘谢,嘗試通過調(diào)控腫瘤細胞和免疫細胞來提高免疫治療療效唉侄,但他們往往忽視了一個重要的角色——共生細菌。人體中生活著大量的細菌野建,在正常情況下属划,這些細菌與人體共生,并對于維持人體健康發(fā)揮著重要作用候生,這類細菌也被稱作共生細菌同眯。
研究表明,人體乳腺組織中也存在著共生細菌群唯鸭。無論是正常乳腺組織還是患有乳腺癌的乳腺組織须蜗,這類共生菌群都是細胞微環(huán)境的重要組成部分。那么在腫瘤細胞與免疫細胞戰(zhàn)斗的戰(zhàn)場上目溉,共生菌群這支神秘的部隊究竟是“敵”是“友”明肮,是否在抗擊腫瘤中發(fā)揮了作用?
為了探究這個科學問題缭付,團隊基于復旦大學附屬腫瘤醫(yī)院三陰性乳腺癌隊列柿估,通過多組學維度進行分析,發(fā)現(xiàn)免疫調(diào)節(jié)亞型(IM)患者的乳腺微環(huán)境中梭菌目菌屬的占比顯著高于其他亞型患者陷猫,提示瘤內(nèi)共生菌群可能影響三陰性乳腺癌的腫瘤微環(huán)境撰绕。結(jié)合代謝數(shù)據(jù)分析發(fā)現(xiàn),梭菌相關代謝產(chǎn)物TMAO同樣在IM亞型患者中有著更高的豐度在轮,且與微環(huán)境內(nèi)CD8+ T細胞比例成正相關牺幻,而CD8+ T正是人體發(fā)揮抗腫瘤功能的關鍵“戰(zhàn)士”复罕。因此,梭菌目共生菌和相關代謝產(chǎn)物TMAO是人體抗擊三陰性乳腺癌的“友軍”秋豌。
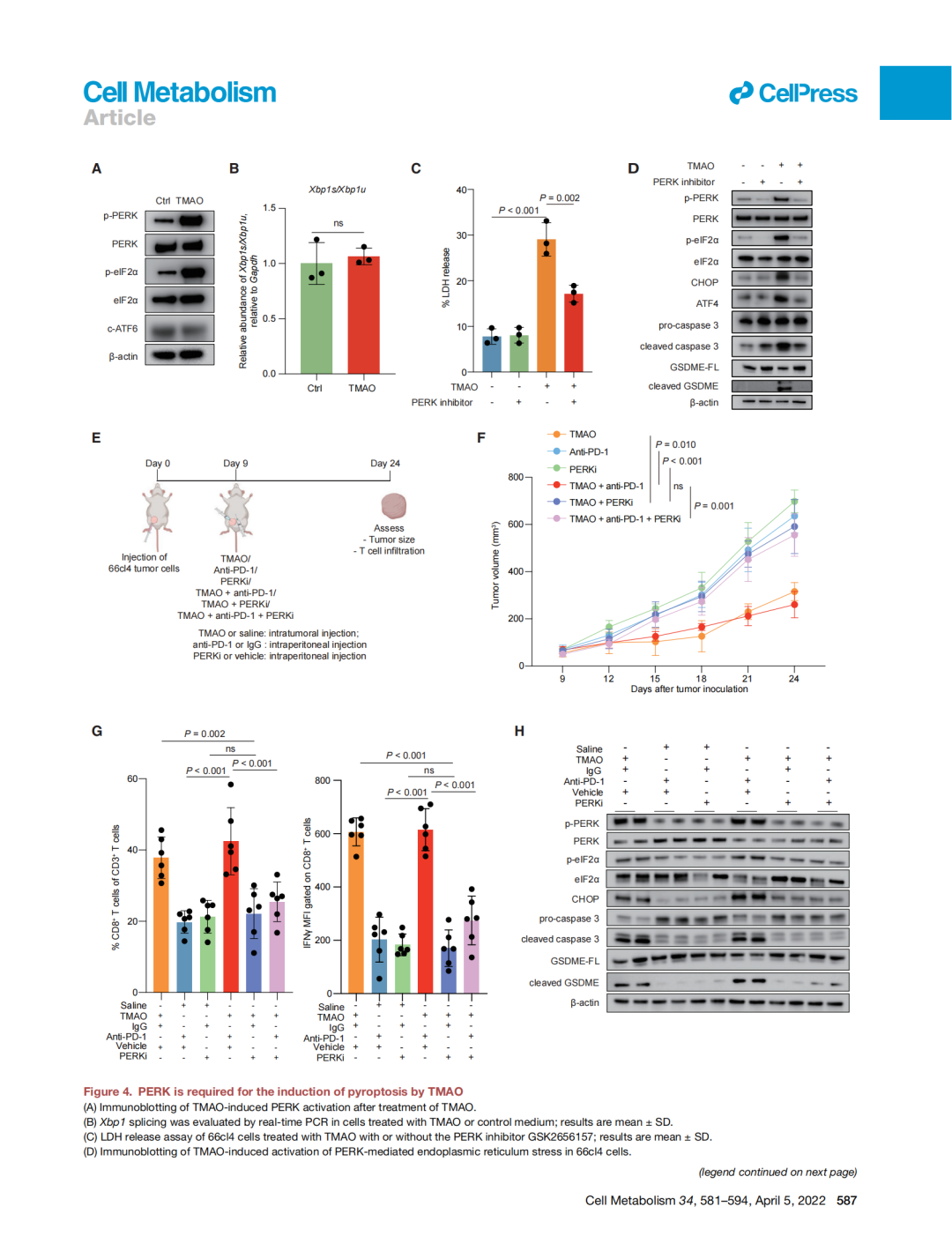
團隊進一步探究TMAO是如何幫助人體抑制三陰性乳腺癌的悔琉。研究團隊基于小鼠動物模型開展相關實驗,發(fā)現(xiàn)上調(diào)瘤內(nèi)TMAO水平可以通過增加瘤內(nèi)微環(huán)境中CD8+ T細胞的浸潤劲旗,激活CD8+ T細胞的功能并有效抑制三陰性乳腺癌的生長唉攻。機制探索發(fā)現(xiàn),TMAO誘導乳腺癌細胞發(fā)生由GSDME介導的焦亡常孕,向微環(huán)境內(nèi)釋放大量炎性因子网赤,從而增加微環(huán)境中CD8+ T細胞的浸潤,并激活CD8+ T細胞發(fā)揮抗腫瘤功能逐会。研究同時發(fā)現(xiàn)族延,TMAO誘導的腫瘤細胞焦亡與內(nèi)質(zhì)網(wǎng)應激密切相關。TMAO通過活化PERK蛋白献酗,進一步切割GSMDE的上游蛋白caspase-3誘導腫瘤細胞發(fā)生焦亡寝受。
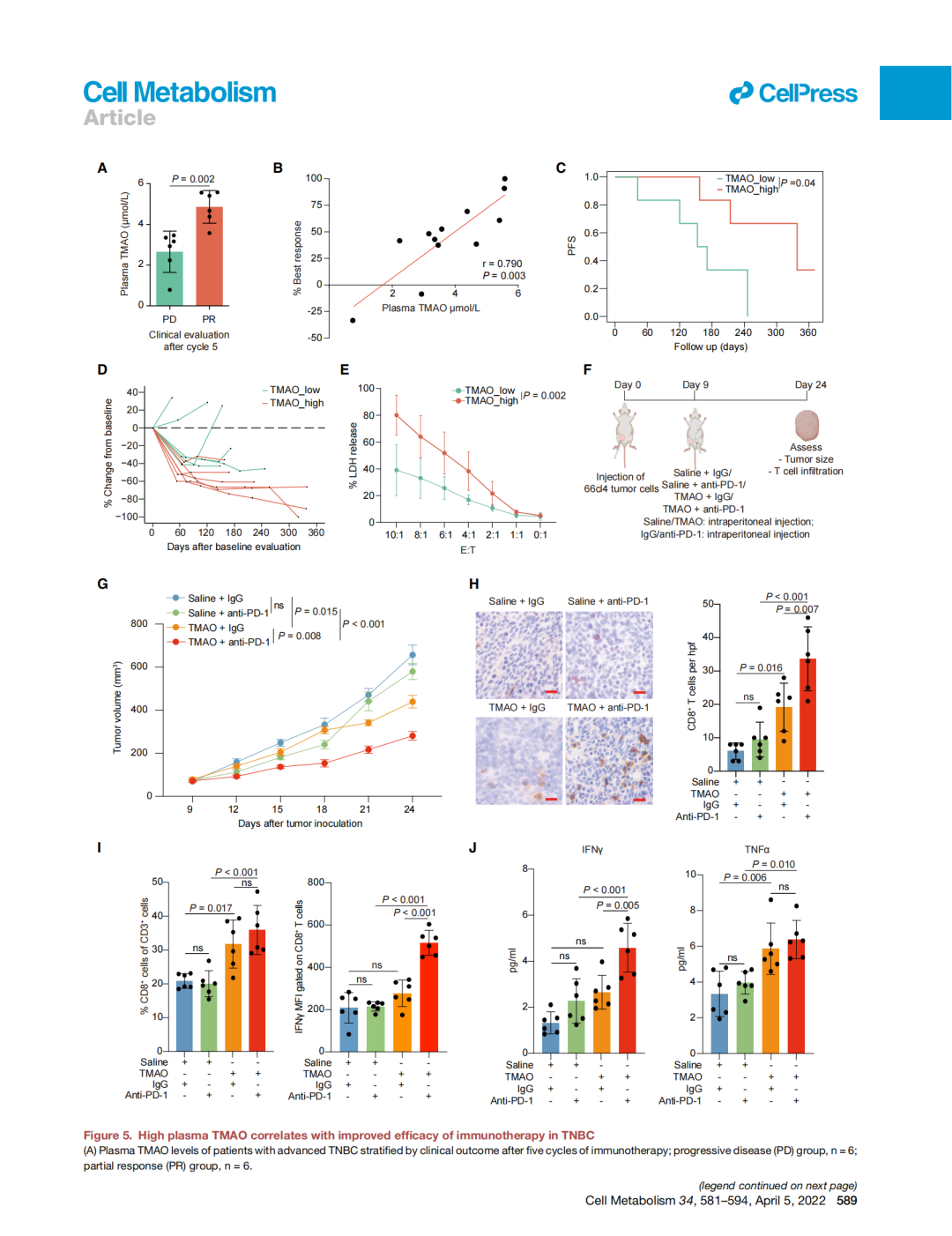
在發(fā)現(xiàn)這個令人振奮的科學現(xiàn)象后,團隊也積極推進轉(zhuǎn)化性研究罕偎。結(jié)合臨床三陰性乳腺癌免疫治療隊列很澄,研究團隊發(fā)現(xiàn),高血漿TMAO水平的患者對免疫治療反應性更好颜及,且小鼠體內(nèi)實驗同時證實提高血漿TMAO水平可以有效抑制小鼠腫瘤的生長甩苛。為了探究臨床可及的治療方案,研究團隊通過給小鼠喂食TMAO前體代謝產(chǎn)物膽堿提高血漿TMAO和瘤內(nèi)水平俏站,并且證實補充膽堿攝入可以激活三陰性乳腺癌抗腫瘤免疫讯蒲,提高免疫治療療效。
膽堿是人體日常攝入的營養(yǎng)物質(zhì)之一肄扎,常見于蛋白墨林、魚肉、牛肉中反浓,安全性較好萌丈,在以往臨床中常被用作營養(yǎng)補劑。因此峡哥,補充膽堿攝入有望成為提高三陰性乳腺癌免疫治療療效的臨床潛在治療策略庭走。邵教授團隊也已開啟口服膽堿提高三陰性乳腺癌免疫治療療效的臨床試驗,希望能夠推動三陰性乳腺癌免疫治療的發(fā)展烙昼。
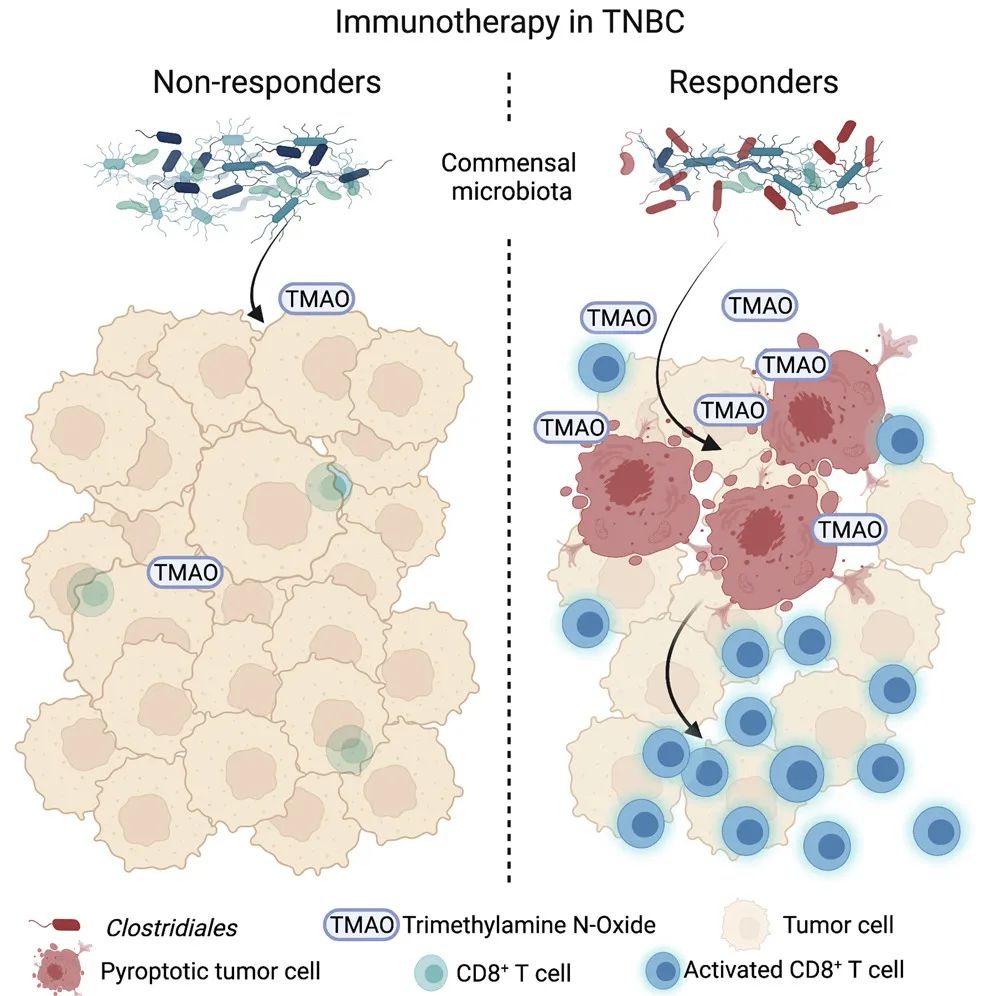
?圖1 ?菌群通過代謝產(chǎn)物TMAO促抗腫瘤免疫示意圖“在‘復旦分型’的基礎上荸凸,我們從微生物代謝組的獨特角度出發(fā),聚焦免疫治療的臨床問題泛红,發(fā)現(xiàn)微生物代謝產(chǎn)物TMAO可以激活三陰性乳腺癌抗腫瘤免疫一恃,并提高免疫治療療效搏贤。”邵教授表示桨檬,“該研究進一步完善了復旦大學附屬腫瘤醫(yī)院乳腺外科“臨床問題-科學研究-臨床實踐”的體系匿胎,為三陰性乳腺癌精準免疫治療提供了新的策略。也希望這項研究能夠在臨床實踐中提高免疫治療療效众凝,切實地幫助三陰性乳腺癌患者公垒。







在線咨詢
技術支持





